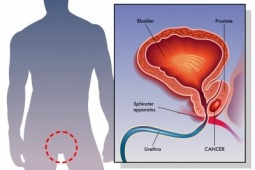
Aflibercept – zawiedzione nadzieje w leczeniu raka prostaty.
Autor:
Dr Mackiewicz
Data: 21.07.2013
Źródło: Tannock I. et al. “Double-blind randomized trial of aflibercept versus placebo with docetaxel and prednisone for treatment of metastatic castration-resistant prostate cancer (mCRPC).” J Clin Oncol 31, 2013 (suppl; abstr 5002)
Podczas corocznego spotkania ASCO (American Society of Clinical Oncology) 2013 zaprezentowano wyniki badania III fazy VENICE oceniającego skuteczność afliberceptu skojarzonego ze standardową terapią u chorych na przerzutowego, opornego na kastrację raka gruczołu krokowego.
Artykuł dostępny wyłącznie dla:
lekarz, lekarz dentysta, lekarz w trakcie specjalizacji.
lekarz, lekarz dentysta, lekarz w trakcie specjalizacji.
Zaloguj się, aby przeczytać pełną treść artykułu.
|
Nie mam jeszcze konta
Utwórz darmowe konto Termedia.
Zarejestruj się
|
Nie pamiętam hasła
Skorzystaj z opcji przypominania hasła aby odzyskać dostęp do swojego konta Termedia.
Nie pamiętam hasła
|