Zgon pacjenta w wyniku omyłkowego podania pankuronium

Pankuronium jest silnym środkiem zwiotczającym mięśnie poprzecznie prążkowane – oprócz zastosowań w anestezjologii i intensywnej terapii jest używany podczas egzekucji jako składnik tzw. zastrzyku śmierci. W praktyce medyczno-sądowej spotyka się przypadki stosowania tej substancji w celu popełnienia samobójstwa lub pozbawienia życia innych osób. Przypadkowe zatrucia są bardzo rzadkie – opisujemy jednak taki przypadek.
Artykuł Rafała Skowronka, Małgorzaty Korczyńskiej, Joanny Kulikowskiej, Joanny Nowickiej, Stanisławy Kabiesz-Neniczki z Katedry i Zakład Medycyny Sądowej i Toksykologii Sądowo-Lekarskiej Wydziału Lekarskiego w Katowicach Śląskiego Uniwersytetu Medycznego:
Pankuronium jest typowym niedepolaryzującym, kuraromimetycznym, silnym środkiem zwiotczającym mięśnie poprzecznie prążkowane na skutek blokady przewodnictwa nerwowo-mięśniowego w płytce motorycznej (ruchowej) na poziomie receptora acetylocholinowego („fałszywy przekaźnik”). Najczęściej jest wykorzystywany w trakcie intubacji pacjenta i prowadzenia oddechu zastępczego podczas znieczulenia ogólnego1. Hamuje układ przywspółczulny, a pobudza współczulny, co objawia się wzrostem częstości akcji serca i wzrostem ciśnienia tętniczego krwi. W przeciwieństwie do swego prekursora – kurary, nie uwalnia histaminy.
Oprócz zastosowań typowo medycznych, w Stanach Zjednoczonych jest używany podczas egzekucji więźniów jako składnik tzw. zastrzyku śmierci2. W praktyce medyczno-sądowej spotyka się przypadki stosowania tej substancji w celu popełnienia samobójstwa lub też w celu pozbawienia życia innych osób. Sprawcami są najczęściej pracownicy szpitali i aptek, co wynika z większej dostępności do farmaceutyków3. Śmierć jest wynikiem uduszenia wskutek zwiotczenia mięśni szkieletowych spowodowanego działaniem leku, przy zachowanej świadomości („chemiczna” asfiksja).
W polskich mediach pankuronium zyskało rozgłos na skutek tzw. afery łowców skór, w której czterem pracownikom łódzkiego pogotowia ratunkowego (dwóm sanitariuszom i dwóm lekarzom) udowodniono udział w zabójstwie pacjentów przy użyciu preparatu Pavulon (prawomocny wyrok Sądu Apelacyjnego w Łodzi z 9 czerwca 2008 r.). Natomiast w mediach zagranicznych popularna była sprawa „anioła śmierci” – terapeuty oddechowego, który aplikował pankuronium swoim podopiecznym4. Przypadkowe zatrucia są niezwykle rzadkie. Autorom pracy udało się znaleźć tylko jedno doniesienie w dostępnej literaturze5.
Cel pracy
Celem niniejszej pracy jest prezentacja rzadkiego przypadku omyłkowego podania pankuronium pacjentowi, w wyniku czego doszło do jego zgonu, oraz przegląd piśmiennictwa dotyczącego przypadków przedawkowania tego leku.
Opis przypadku
57-letnia kobieta, alkoholiczka, została przyjęta na oddział toksykologii klinicznej w regionalnym ośrodku ostrych zatruć po wypiciu preparatu zawierającego glikol etylenowy (prawdopodobnie płynu do odmrażania szyb lub płynu do chłodnic samochodowych).
Badania biochemiczne ujawniły kwasicę metaboliczną i niewydolność nerek, natomiast badania obrazowe (tomografia komputerowa) – zmianę w okolicy czołowej mogącą odpowiadać oponiakowi. W analizie toksykologicznej wykonanej w laboratorium klinicznym stwierdzono obecność glikolu etylenowego w stężeniach: we krwi – 9,63 mg/dl, a w moczu – 9100,4 mg/dl.
Na podstawie wywiadu, badania fizykalnego i wyników badań dodatkowych rozpoznano zatrucie glikolem etylenowym z następczą ostrą niewydolnością nerek. Dodatkowo stwierdzono zespół zależności alkoholowej, chorobę niedokrwienną serca, nadciśnienie tętnicze i stan po cholecystektomii.
Terapeutycznie zastosowano etanol, 8,4 proc. wodorowęglan sodu, 20 proc. mannitol, chlorek potasu (dożylnie), glukonian wapnia, metoklopramid, furosemid, ranitydynę, cefotaksym i preparaty zawierające witaminy. W ciągu 10 godzin uzyskano normalizację parametrów gospodarki kwasowo-zasadowej i eliminację glikolu etylenowego z krwi. Pacjentka była przytomna. W ciągu następnych 24 godzin wystąpił epizod ostrej niewydolności nerek ze skąpomoczem, który leczono między innymi wysokimi dawkami furosemidu. W trzeciej dobie hospitalizacji pojawiły się omamy związane z zespołem odstawiennym, podano więc promazynę i haloperidol. We krwi stwierdzono wzrost stężenia kreatyniny. W piątej dobie doszło do nagłego zatrzymania oddechu i krążenia. Podjęto czynności resuscytacyjne, pacjentka została zaintubowana. Mimo tego po 1 godzinie i 45 minutach działań ratunkowych stwierdzono zgon.
Pierwotnie za przyczynę zgonu przyjęto ostre zatrucie glikolem etylenowym z następczą ostrą niewydolnością nerek. Pod uwagę brano również nagłą śmierć sercową (pacjentka z zaawansowaną chorobą niedokrwienną serca). Jednak ze względu na niejasne tło nagłego pogorszenia stanu klinicznego pacjentki oraz zeznania pielęgniarki, która przyznała, że zamiast furosemidu mogła omyłkowo podać pacjentce pankuronium przeznaczone dla pacjenta znajdującego się na sąsiednim łóżku, wszczęto śledztwo w sprawie nieumyślnego spowodowania śmierci. Prokurator zlecił przeprowadzenie sądowo-lekarskiej sekcji zwłok oraz dalsze niezbędne badania dodatkowe (histopatologiczne i chemiczno-toksykologiczne).
Sekcja zwłok ujawniła podbiegnięcia krwawe na kończynach dolnych oraz wkłucia po iniekcjach jako ślady interwencji medycznych. Ze zmian chorobowych stwierdzono: przekrwienie i obrzęk mózgu, widoczne zgrubienie opony miękkiej między płatami czołowymi, obrzęk płuc, miażdżycę naczyń wieńcowych, zmiany degeneracyjne w mięśniu sercowym oraz poszerzenie jam serca, zwyrodnienie tłuszczowe wątroby, stan po cholecystektomii, cechy ostrej niewydolności nerek i zwłóknienie trzustki. Obraz makroskopowy był więc niecharakterystyczny.
W badaniach histopatologicznych stwierdzono:
– w sercu – wysokiego stopnia miażdżycę naczyń wieńcowych i hipertrofię mięśnia sercowego z niewielkimi bliznami pozawałowymi,
– w nerkach – przekrwienie, ogniskowe śródmiąższowe nacieki zapalne i zwyrodnienie wodniczkowe nabłonka kory nerek,
– w wątrobie – rozsiane drobnokropelkowe zwyrodnienie tłuszczowe; w płucach – obrzęk z zastojem, rozedmę i ogniska pylicy węglowej.
Zabezpieczony podczas sekcji zwłok materiał biologiczny poddano badaniom chemiczno-toksykologicznym. Próbkę krwi oraz wycinki wątroby i nerki badano metodą chromatografii gazowej – techniką analizy fazy nadpowierzchniowej (headspace) i techniką analizy prób płynnych w kierunku obecności alkoholi niekonsumpcyjnych, takich jak: alkohol metylowy, alkohol izopropylowy, glikol etylenowy i glikol propylenowy, oraz ich metabolitów – kwasu mrówkowego, acetonu, aldehydu glikolowego, kwasu glikolowego. Przeprowadzone badania dały wynik ujemny.
Dalsze badania chemiczno-toksykologiczne materiału biologicznego prowadzono w kierunku obecności substancji psychoaktywnych i podstawowych grup leków oraz pankuronium.
Do wyosobnienia substancji psychoaktywnych i leków o charakterze zasadowym z krwi wykorzystano ekstrakcję ciecz–ciecz octanem etylu. Uzyskany wyciąg odparowano, a suchą pozostałość przeniesiono do niewielkiej objętości metanolu. Ekstrakt metanolowy badano metodą chromatografii cieczowej sprzężonej ze spektrometrią mas w trybie jonizacji dodatniej przez rozpylanie w polu elektrycznym (LC-ESI-MS).
Materiał miąższowy analizowano w kierunku obecności leków o charakterze kwaśnym i zasado-wym oraz środków psychoaktywnych. W tym celu próbki wątroby i nerek po rozdrobnieniu, odbiałczeniu i przesączeniu do fazy wodnej ekstrahowano eterem ze środowiska kwaśnego, a następnie chloroformem ze środowiska zasadowego. Otrzymane ekstrakty organiczne badano metodą chromatografii cienkowarstwowej (TLC) na żelu krzemionkowym G naniesionym na płytki z folii aluminiowej oraz metodą LC-ESI-MS.
Ze względu na charakter chemiczny pankuronium do jego identyfikacji zastosowano specjalne postępowanie analityczne 5. Lek ten zalicza się do czwartorzędowych soli amoniowych, które w roztworach wodnych pozostają zdysocjowane w całym zakresie pH, co praktycznie uniemożliwia ekstrakcję rozpuszczalnikami organicznymi. Metodą z wyboru izolacji tej substancji z materiału biologicznego jest ekstrakcja z przeciwjonem (ion-pair extraction).
Krew zadano więc nasyconym roztworem jodku potasu i buforem fosforanowym o pH = 5, a następnie przeprowadzono ekstrakcję za pomocą chlorku metylenu. Uzyskany wyciąg odparowano, a pozostałość przeniesiono do małej, ściśle określonej objętości metanolu. Ekstrakt metanolowy badano metodą LC-ESI-MS. W ten sam sposób przeprowadzono analizę „ślepej” próbki krwi, tzn. próbki, w której wcześniej wykluczono obecność leków, i „ślepej” próbki krwi z dodanym wzorcem pankuronium.
Wyniki badań chemiczno-toksykologicznych materiału biologicznego zabezpieczonego podczas sekcji zwłok przedstawiono w tabeli I.

W analizowanym materiale oznaczono pankuronium we krwi oraz potwierdzono obecność podawanych pacjentce w czasie hospitalizacji leków, to jest metoklopramidu, aminofenazonu i furosemidu. Stężenie we krwi me-toklopramidu i aminofenazonu mieściło się w zakresie stężeń terapeutycznych.
Biorąc pod uwagę całość przeprowadzonych badań, czyli badania sekcyjnego, histopatologicznego i chemiczno-toksykologicznego, a także informacje zawarte w karcie leczenia szpitalnego i notatce służbowej, stwierdzono, iż zgon 57-letniej pacjentki obciążonej przewlekłą chorobą niedokrwienną serca, w trakcie leczenia z powodu zatrucia niekonsumpcyjnym alkoholem (glikolem etylenowym) z następową ostrą niewydolnością nerek, nastąpił na skutek nagłego zatrzymania oddechu i krążenia w następstwie omyłkowego podania pankuronium.
Prokurator zażądał dla pielęgniarki kary 2 lat pozbawienia wolności w zawieszeniu na okres wynoszący 5 lat oraz zakaz wykonywania zawodu przez 2 lata. Ostatecznie sąd rejonowy uznał ją winną nieumyślnego spowodowania śmierci pacjenta (art. 155 k.k.) i orzekł karę pozbawienia wolności na okres 1 roku i 6 miesięcy w zawieszeniu na okres próby wynoszący 4 lata.
Dyskusja
Pankuronium jest aminosteroidem podawanym jako dibromek w dawkach: przy intubacji – 0,08 do 0,10 mg/kg, a przy wstępnej kuraryzacji – 0,01 do 0,02 mg/kg 1. Jego stężenie terapeutyczne zawiera się w granicach 200–600 ng/ml 6. Stężenia stwierdzane w przypadkach przedawkowania wraz z ich krótką charakterystyką zebrano w tabeli II 5–11.
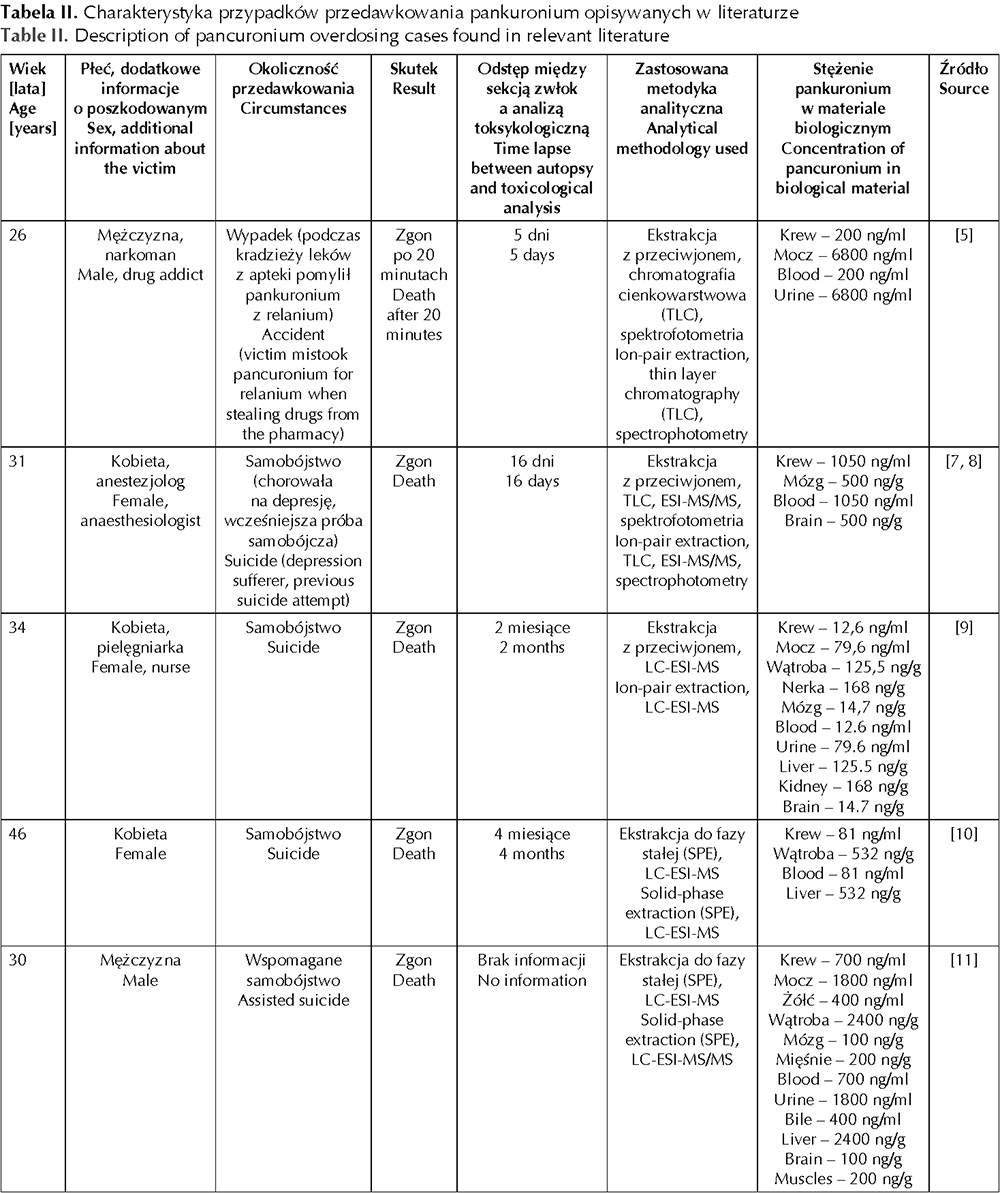
W omawianym przypadku odnotowane stężenie – 190 ng/ml – było stężeniem terapeutycznym. Jednakże każda skuteczna dawka pankuronium, tzn. powodująca zwiotczenie mięśni szkieletowych, podana pacjentowi, którego oddech nie jest wspomagany i – co najważniejsze – nie jest monitorowany, może stanowić zagrożenie dla jego życia, jeśli nie zostanie udzielona natychmiastowa pomoc.
W takich przypadkach, oprócz natychmiastowego udrożnienia dróg oddechowych i rozpoczęcia oddechu zastępczego, należy rozważyć podanie odpowiednich odtrutek. Mogą to być leki z grupy inhibitorów acetylocholinoesterazy, na przykład neostygmina, atropina czy niedawno wprowadzony na rynek sugammadeks, czyli zmodyfikowana γ-cyklodekstryna, wybiórczo opłaszczająca i inaktywująca leki zwiotczające, tym samym odwracająca blokadę przewodnictwa nerwowo-mięśniowego (selective relaxant binding agent)1, 12.
Co prawda ten ostatni lek jest przeznaczony do odwracania działania rokuronium i wekuronium, lecz potwierdzono jego skuteczność również w odniesieniu do pankuronium13.
Dodatkowym niekorzystnym czynnikiem w prezentowanym przez nas przypadku, zwiększającym ekspozycję na pankuronium, była z pewnością niewydolność nerek na tle ich toksycznego uszkodzenia metabolitami glikolu etylenowego. Nerki są najważniejszym narządem eliminacji pankuronium – ok. 37–44 proc. podanej dawki jest wydalane w postaci niezmienionej, a ok. 15 proc. jako 3-hydroksy metabolity14. Dlatego też niewydolność tego narządu jest traktowana jako względne przeciwwskazanie do stosowania leku, co wymusza zmniejszenie dawki lub zastąpienie go innym niedepolaryzującym środkiem zwiotczającym1.
Omyłkowe podania leków i innych środków medycznych mogą polegać na podaniu niewłaściwej substancji lub właściwej substancji w niewłaściwy sposób (np. w nieodpowiedniej dawce czy stężeniu). W tego typu sytuacjach klinicznych kluczowe jest szybkie rozpoznanie i wdrożenie procedur mających na celu zapobieżenie powikłaniom. Przykładem może być przypadek omyłkowego, dożylnego podania formaliny zaprezentowany przez Smędrę-Kaźmirską i wsp.15. Po rozpoznaniu błędu w warunkach sali operacyjnej chorego przeniesiono na oddział intensywnej terapii, dokonano intubacji tchawicy, rozpoczęto mechaniczną wentylację płuc oraz sześciogodzinną hemodializę, co zapobiegło potencjalnym powikłaniom. Niestety niektóre przypadki omyłkowego podania środków medycznych, mimo udzielonej pomocy, kończą się zgonem pacjenta.
Na koniec należy jeszcze zwrócić uwagę na konieczność profilaktyki błędów medycznych oraz stałej edukacji personelu lekarskiego i pielęgniarskiego. Bezsprzecznie w przedstawionym przez nas przypadku zaistniał błąd medyczny o charakterze tzw. błędu wykonawczego. Pielęgniarka nie zachowała należnej staranności. Przed podaniem leku powinna sprawdzić zawartość fiolki i tożsamość pacjenta, aby upewnić się, że podaje właściwy lek właściwej osobie. Celowe wydaje się wypracowanie procedur zgłaszania i postępowania w przypadkach omyłkowego podania leków, zwłaszcza w odniesieniu do często stosowanych w anestezjologii i intensywnej terapii grup leków, których niewłaściwe zastosowanie może stanowić zagrożenie dla zdrowia i życia pacjenta.
Piśmiennictwo:
1. Flake F, Lutomsky B. Leki w medycynie ratunkowej i intensywnej terapii. Urban & Partner, Wrocław 2003; 171-172.
2. Zimmers TA, Sheldon J, Lubarsky DA, Lopez-Munoz F, Waterman L, Weisman R, Koniaris LG. Lethal Injection for Execution: Chemical Asphyxiation? PLoS Med 2007; 4: 646-653.
3. Johnstone RE, Katz RL, Stanley TH. Homicides using muscle relaxants, opioids, and anesthetic drugs: anesthesiologist assistance in their investigation and prosecution. Anesthesiology 2011; 114: 713-716.
4. Andresen BD, Alcaraz A, Grant PM. The application of pancuronium bromide (Pavulon) forensic analyses to tissue samples from an “Angel of Death” investigation. J Forensic Sci 2005; 50: 215-219.
5. Kłys M, Baran E. Przypadek śmiertelnego zatrucia Pavulonem. Arch Med Sadowej Kryminol 1987; 37: 247-251.
6. Schulz M, Schmoldt A. Therapeutic and toxic blood concentrations of more than 500 drugs. Pharmazie 1997; 52: 895-911.
7. Kłys M, Białka J, Bujak-Giżycka B. A case of suicide by intravenous injection of pancuronium. Leg Med 2000; 2: 93-100.
8. Kłys M, Bujak-Giżycka B. Zastosowanie chromatografii cieczowej z detekcją masową (LC/MS) w ekspertyzie toksykologicznej. Arch Med Sadowej Kryminol 2000; 50: 115-126.
9. Pufal E, Sykutera M, Rochholz G, Śliwka K. Determination of pancuronium in biological fluids and organ samples. Probl Forensic Sci 2007; 72: 450-457.
10. Kała M, Lechowicz W. Instability of pancuronium in postmortem blood and liver taken after a fatal intramuscular Pavulon injection. Forensic Sci Int 2004; 143: 191-198.
11. Kerskes CHM, Lusthof KJ, Zweipfenning PGM, Franke P. The detection and identification of quaternary nitrogen muscle relaxants in biological fluids and tissues by ion-trap LC-ESI-MS. J Anal Toxicol 2002; 26: 29-34.
12. Glinka L, Onichimowski D, Sieniuta P, Korecki A. Dwa lata doświadczeń z zastosowaniem sugammadeksu w praktyce klinicznej. Anestezjologia Intensywna Terapia 2010; 42: 155-159.
13. Decoopman M, Cammu G, Suy K, Heeringa M, Demeyer I. Reversal of pancuronium-induced block by the selective relaxant binding agent sugammadex: 9AP2-1. Eur J Anaesthesiol 2007; 24: 110-111.
14. Moffat AC, Osselton MD, Widdop B. Clarke’s analysis of drugs and poisons in pharmaceuticals, body fluids and postmortem material. Fourth edition. Pharmaceutical Press, London 2011; 1853-1854.
15. Smędra-Kaźmirska A, Żydek L, Barzdo M, Machała W, Berent J. Omyłkowe dożylne podanie roztworu formaliny. Anestezjologia Intensywna Terapia 2009; 41: 163-165.
Artykuł opublikowano w „Archiwum Medycyny Sądowej i Kryminologii” 4/2017.

Pankuronium jest typowym niedepolaryzującym, kuraromimetycznym, silnym środkiem zwiotczającym mięśnie poprzecznie prążkowane na skutek blokady przewodnictwa nerwowo-mięśniowego w płytce motorycznej (ruchowej) na poziomie receptora acetylocholinowego („fałszywy przekaźnik”). Najczęściej jest wykorzystywany w trakcie intubacji pacjenta i prowadzenia oddechu zastępczego podczas znieczulenia ogólnego1. Hamuje układ przywspółczulny, a pobudza współczulny, co objawia się wzrostem częstości akcji serca i wzrostem ciśnienia tętniczego krwi. W przeciwieństwie do swego prekursora – kurary, nie uwalnia histaminy.
Oprócz zastosowań typowo medycznych, w Stanach Zjednoczonych jest używany podczas egzekucji więźniów jako składnik tzw. zastrzyku śmierci2. W praktyce medyczno-sądowej spotyka się przypadki stosowania tej substancji w celu popełnienia samobójstwa lub też w celu pozbawienia życia innych osób. Sprawcami są najczęściej pracownicy szpitali i aptek, co wynika z większej dostępności do farmaceutyków3. Śmierć jest wynikiem uduszenia wskutek zwiotczenia mięśni szkieletowych spowodowanego działaniem leku, przy zachowanej świadomości („chemiczna” asfiksja).
W polskich mediach pankuronium zyskało rozgłos na skutek tzw. afery łowców skór, w której czterem pracownikom łódzkiego pogotowia ratunkowego (dwóm sanitariuszom i dwóm lekarzom) udowodniono udział w zabójstwie pacjentów przy użyciu preparatu Pavulon (prawomocny wyrok Sądu Apelacyjnego w Łodzi z 9 czerwca 2008 r.). Natomiast w mediach zagranicznych popularna była sprawa „anioła śmierci” – terapeuty oddechowego, który aplikował pankuronium swoim podopiecznym4. Przypadkowe zatrucia są niezwykle rzadkie. Autorom pracy udało się znaleźć tylko jedno doniesienie w dostępnej literaturze5.
Cel pracy
Celem niniejszej pracy jest prezentacja rzadkiego przypadku omyłkowego podania pankuronium pacjentowi, w wyniku czego doszło do jego zgonu, oraz przegląd piśmiennictwa dotyczącego przypadków przedawkowania tego leku.
Opis przypadku
57-letnia kobieta, alkoholiczka, została przyjęta na oddział toksykologii klinicznej w regionalnym ośrodku ostrych zatruć po wypiciu preparatu zawierającego glikol etylenowy (prawdopodobnie płynu do odmrażania szyb lub płynu do chłodnic samochodowych).
Badania biochemiczne ujawniły kwasicę metaboliczną i niewydolność nerek, natomiast badania obrazowe (tomografia komputerowa) – zmianę w okolicy czołowej mogącą odpowiadać oponiakowi. W analizie toksykologicznej wykonanej w laboratorium klinicznym stwierdzono obecność glikolu etylenowego w stężeniach: we krwi – 9,63 mg/dl, a w moczu – 9100,4 mg/dl.
Na podstawie wywiadu, badania fizykalnego i wyników badań dodatkowych rozpoznano zatrucie glikolem etylenowym z następczą ostrą niewydolnością nerek. Dodatkowo stwierdzono zespół zależności alkoholowej, chorobę niedokrwienną serca, nadciśnienie tętnicze i stan po cholecystektomii.
Terapeutycznie zastosowano etanol, 8,4 proc. wodorowęglan sodu, 20 proc. mannitol, chlorek potasu (dożylnie), glukonian wapnia, metoklopramid, furosemid, ranitydynę, cefotaksym i preparaty zawierające witaminy. W ciągu 10 godzin uzyskano normalizację parametrów gospodarki kwasowo-zasadowej i eliminację glikolu etylenowego z krwi. Pacjentka była przytomna. W ciągu następnych 24 godzin wystąpił epizod ostrej niewydolności nerek ze skąpomoczem, który leczono między innymi wysokimi dawkami furosemidu. W trzeciej dobie hospitalizacji pojawiły się omamy związane z zespołem odstawiennym, podano więc promazynę i haloperidol. We krwi stwierdzono wzrost stężenia kreatyniny. W piątej dobie doszło do nagłego zatrzymania oddechu i krążenia. Podjęto czynności resuscytacyjne, pacjentka została zaintubowana. Mimo tego po 1 godzinie i 45 minutach działań ratunkowych stwierdzono zgon.
Pierwotnie za przyczynę zgonu przyjęto ostre zatrucie glikolem etylenowym z następczą ostrą niewydolnością nerek. Pod uwagę brano również nagłą śmierć sercową (pacjentka z zaawansowaną chorobą niedokrwienną serca). Jednak ze względu na niejasne tło nagłego pogorszenia stanu klinicznego pacjentki oraz zeznania pielęgniarki, która przyznała, że zamiast furosemidu mogła omyłkowo podać pacjentce pankuronium przeznaczone dla pacjenta znajdującego się na sąsiednim łóżku, wszczęto śledztwo w sprawie nieumyślnego spowodowania śmierci. Prokurator zlecił przeprowadzenie sądowo-lekarskiej sekcji zwłok oraz dalsze niezbędne badania dodatkowe (histopatologiczne i chemiczno-toksykologiczne).
Sekcja zwłok ujawniła podbiegnięcia krwawe na kończynach dolnych oraz wkłucia po iniekcjach jako ślady interwencji medycznych. Ze zmian chorobowych stwierdzono: przekrwienie i obrzęk mózgu, widoczne zgrubienie opony miękkiej między płatami czołowymi, obrzęk płuc, miażdżycę naczyń wieńcowych, zmiany degeneracyjne w mięśniu sercowym oraz poszerzenie jam serca, zwyrodnienie tłuszczowe wątroby, stan po cholecystektomii, cechy ostrej niewydolności nerek i zwłóknienie trzustki. Obraz makroskopowy był więc niecharakterystyczny.
W badaniach histopatologicznych stwierdzono:
– w sercu – wysokiego stopnia miażdżycę naczyń wieńcowych i hipertrofię mięśnia sercowego z niewielkimi bliznami pozawałowymi,
– w nerkach – przekrwienie, ogniskowe śródmiąższowe nacieki zapalne i zwyrodnienie wodniczkowe nabłonka kory nerek,
– w wątrobie – rozsiane drobnokropelkowe zwyrodnienie tłuszczowe; w płucach – obrzęk z zastojem, rozedmę i ogniska pylicy węglowej.
Zabezpieczony podczas sekcji zwłok materiał biologiczny poddano badaniom chemiczno-toksykologicznym. Próbkę krwi oraz wycinki wątroby i nerki badano metodą chromatografii gazowej – techniką analizy fazy nadpowierzchniowej (headspace) i techniką analizy prób płynnych w kierunku obecności alkoholi niekonsumpcyjnych, takich jak: alkohol metylowy, alkohol izopropylowy, glikol etylenowy i glikol propylenowy, oraz ich metabolitów – kwasu mrówkowego, acetonu, aldehydu glikolowego, kwasu glikolowego. Przeprowadzone badania dały wynik ujemny.
Dalsze badania chemiczno-toksykologiczne materiału biologicznego prowadzono w kierunku obecności substancji psychoaktywnych i podstawowych grup leków oraz pankuronium.
Do wyosobnienia substancji psychoaktywnych i leków o charakterze zasadowym z krwi wykorzystano ekstrakcję ciecz–ciecz octanem etylu. Uzyskany wyciąg odparowano, a suchą pozostałość przeniesiono do niewielkiej objętości metanolu. Ekstrakt metanolowy badano metodą chromatografii cieczowej sprzężonej ze spektrometrią mas w trybie jonizacji dodatniej przez rozpylanie w polu elektrycznym (LC-ESI-MS).
Materiał miąższowy analizowano w kierunku obecności leków o charakterze kwaśnym i zasado-wym oraz środków psychoaktywnych. W tym celu próbki wątroby i nerek po rozdrobnieniu, odbiałczeniu i przesączeniu do fazy wodnej ekstrahowano eterem ze środowiska kwaśnego, a następnie chloroformem ze środowiska zasadowego. Otrzymane ekstrakty organiczne badano metodą chromatografii cienkowarstwowej (TLC) na żelu krzemionkowym G naniesionym na płytki z folii aluminiowej oraz metodą LC-ESI-MS.
Ze względu na charakter chemiczny pankuronium do jego identyfikacji zastosowano specjalne postępowanie analityczne 5. Lek ten zalicza się do czwartorzędowych soli amoniowych, które w roztworach wodnych pozostają zdysocjowane w całym zakresie pH, co praktycznie uniemożliwia ekstrakcję rozpuszczalnikami organicznymi. Metodą z wyboru izolacji tej substancji z materiału biologicznego jest ekstrakcja z przeciwjonem (ion-pair extraction).
Krew zadano więc nasyconym roztworem jodku potasu i buforem fosforanowym o pH = 5, a następnie przeprowadzono ekstrakcję za pomocą chlorku metylenu. Uzyskany wyciąg odparowano, a pozostałość przeniesiono do małej, ściśle określonej objętości metanolu. Ekstrakt metanolowy badano metodą LC-ESI-MS. W ten sam sposób przeprowadzono analizę „ślepej” próbki krwi, tzn. próbki, w której wcześniej wykluczono obecność leków, i „ślepej” próbki krwi z dodanym wzorcem pankuronium.
Wyniki badań chemiczno-toksykologicznych materiału biologicznego zabezpieczonego podczas sekcji zwłok przedstawiono w tabeli I.

W analizowanym materiale oznaczono pankuronium we krwi oraz potwierdzono obecność podawanych pacjentce w czasie hospitalizacji leków, to jest metoklopramidu, aminofenazonu i furosemidu. Stężenie we krwi me-toklopramidu i aminofenazonu mieściło się w zakresie stężeń terapeutycznych.
Biorąc pod uwagę całość przeprowadzonych badań, czyli badania sekcyjnego, histopatologicznego i chemiczno-toksykologicznego, a także informacje zawarte w karcie leczenia szpitalnego i notatce służbowej, stwierdzono, iż zgon 57-letniej pacjentki obciążonej przewlekłą chorobą niedokrwienną serca, w trakcie leczenia z powodu zatrucia niekonsumpcyjnym alkoholem (glikolem etylenowym) z następową ostrą niewydolnością nerek, nastąpił na skutek nagłego zatrzymania oddechu i krążenia w następstwie omyłkowego podania pankuronium.
Prokurator zażądał dla pielęgniarki kary 2 lat pozbawienia wolności w zawieszeniu na okres wynoszący 5 lat oraz zakaz wykonywania zawodu przez 2 lata. Ostatecznie sąd rejonowy uznał ją winną nieumyślnego spowodowania śmierci pacjenta (art. 155 k.k.) i orzekł karę pozbawienia wolności na okres 1 roku i 6 miesięcy w zawieszeniu na okres próby wynoszący 4 lata.
Dyskusja
Pankuronium jest aminosteroidem podawanym jako dibromek w dawkach: przy intubacji – 0,08 do 0,10 mg/kg, a przy wstępnej kuraryzacji – 0,01 do 0,02 mg/kg 1. Jego stężenie terapeutyczne zawiera się w granicach 200–600 ng/ml 6. Stężenia stwierdzane w przypadkach przedawkowania wraz z ich krótką charakterystyką zebrano w tabeli II 5–11.

W omawianym przypadku odnotowane stężenie – 190 ng/ml – było stężeniem terapeutycznym. Jednakże każda skuteczna dawka pankuronium, tzn. powodująca zwiotczenie mięśni szkieletowych, podana pacjentowi, którego oddech nie jest wspomagany i – co najważniejsze – nie jest monitorowany, może stanowić zagrożenie dla jego życia, jeśli nie zostanie udzielona natychmiastowa pomoc.
W takich przypadkach, oprócz natychmiastowego udrożnienia dróg oddechowych i rozpoczęcia oddechu zastępczego, należy rozważyć podanie odpowiednich odtrutek. Mogą to być leki z grupy inhibitorów acetylocholinoesterazy, na przykład neostygmina, atropina czy niedawno wprowadzony na rynek sugammadeks, czyli zmodyfikowana γ-cyklodekstryna, wybiórczo opłaszczająca i inaktywująca leki zwiotczające, tym samym odwracająca blokadę przewodnictwa nerwowo-mięśniowego (selective relaxant binding agent)1, 12.
Co prawda ten ostatni lek jest przeznaczony do odwracania działania rokuronium i wekuronium, lecz potwierdzono jego skuteczność również w odniesieniu do pankuronium13.
Dodatkowym niekorzystnym czynnikiem w prezentowanym przez nas przypadku, zwiększającym ekspozycję na pankuronium, była z pewnością niewydolność nerek na tle ich toksycznego uszkodzenia metabolitami glikolu etylenowego. Nerki są najważniejszym narządem eliminacji pankuronium – ok. 37–44 proc. podanej dawki jest wydalane w postaci niezmienionej, a ok. 15 proc. jako 3-hydroksy metabolity14. Dlatego też niewydolność tego narządu jest traktowana jako względne przeciwwskazanie do stosowania leku, co wymusza zmniejszenie dawki lub zastąpienie go innym niedepolaryzującym środkiem zwiotczającym1.
Omyłkowe podania leków i innych środków medycznych mogą polegać na podaniu niewłaściwej substancji lub właściwej substancji w niewłaściwy sposób (np. w nieodpowiedniej dawce czy stężeniu). W tego typu sytuacjach klinicznych kluczowe jest szybkie rozpoznanie i wdrożenie procedur mających na celu zapobieżenie powikłaniom. Przykładem może być przypadek omyłkowego, dożylnego podania formaliny zaprezentowany przez Smędrę-Kaźmirską i wsp.15. Po rozpoznaniu błędu w warunkach sali operacyjnej chorego przeniesiono na oddział intensywnej terapii, dokonano intubacji tchawicy, rozpoczęto mechaniczną wentylację płuc oraz sześciogodzinną hemodializę, co zapobiegło potencjalnym powikłaniom. Niestety niektóre przypadki omyłkowego podania środków medycznych, mimo udzielonej pomocy, kończą się zgonem pacjenta.
Na koniec należy jeszcze zwrócić uwagę na konieczność profilaktyki błędów medycznych oraz stałej edukacji personelu lekarskiego i pielęgniarskiego. Bezsprzecznie w przedstawionym przez nas przypadku zaistniał błąd medyczny o charakterze tzw. błędu wykonawczego. Pielęgniarka nie zachowała należnej staranności. Przed podaniem leku powinna sprawdzić zawartość fiolki i tożsamość pacjenta, aby upewnić się, że podaje właściwy lek właściwej osobie. Celowe wydaje się wypracowanie procedur zgłaszania i postępowania w przypadkach omyłkowego podania leków, zwłaszcza w odniesieniu do często stosowanych w anestezjologii i intensywnej terapii grup leków, których niewłaściwe zastosowanie może stanowić zagrożenie dla zdrowia i życia pacjenta.
Piśmiennictwo:
1. Flake F, Lutomsky B. Leki w medycynie ratunkowej i intensywnej terapii. Urban & Partner, Wrocław 2003; 171-172.
2. Zimmers TA, Sheldon J, Lubarsky DA, Lopez-Munoz F, Waterman L, Weisman R, Koniaris LG. Lethal Injection for Execution: Chemical Asphyxiation? PLoS Med 2007; 4: 646-653.
3. Johnstone RE, Katz RL, Stanley TH. Homicides using muscle relaxants, opioids, and anesthetic drugs: anesthesiologist assistance in their investigation and prosecution. Anesthesiology 2011; 114: 713-716.
4. Andresen BD, Alcaraz A, Grant PM. The application of pancuronium bromide (Pavulon) forensic analyses to tissue samples from an “Angel of Death” investigation. J Forensic Sci 2005; 50: 215-219.
5. Kłys M, Baran E. Przypadek śmiertelnego zatrucia Pavulonem. Arch Med Sadowej Kryminol 1987; 37: 247-251.
6. Schulz M, Schmoldt A. Therapeutic and toxic blood concentrations of more than 500 drugs. Pharmazie 1997; 52: 895-911.
7. Kłys M, Białka J, Bujak-Giżycka B. A case of suicide by intravenous injection of pancuronium. Leg Med 2000; 2: 93-100.
8. Kłys M, Bujak-Giżycka B. Zastosowanie chromatografii cieczowej z detekcją masową (LC/MS) w ekspertyzie toksykologicznej. Arch Med Sadowej Kryminol 2000; 50: 115-126.
9. Pufal E, Sykutera M, Rochholz G, Śliwka K. Determination of pancuronium in biological fluids and organ samples. Probl Forensic Sci 2007; 72: 450-457.
10. Kała M, Lechowicz W. Instability of pancuronium in postmortem blood and liver taken after a fatal intramuscular Pavulon injection. Forensic Sci Int 2004; 143: 191-198.
11. Kerskes CHM, Lusthof KJ, Zweipfenning PGM, Franke P. The detection and identification of quaternary nitrogen muscle relaxants in biological fluids and tissues by ion-trap LC-ESI-MS. J Anal Toxicol 2002; 26: 29-34.
12. Glinka L, Onichimowski D, Sieniuta P, Korecki A. Dwa lata doświadczeń z zastosowaniem sugammadeksu w praktyce klinicznej. Anestezjologia Intensywna Terapia 2010; 42: 155-159.
13. Decoopman M, Cammu G, Suy K, Heeringa M, Demeyer I. Reversal of pancuronium-induced block by the selective relaxant binding agent sugammadex: 9AP2-1. Eur J Anaesthesiol 2007; 24: 110-111.
14. Moffat AC, Osselton MD, Widdop B. Clarke’s analysis of drugs and poisons in pharmaceuticals, body fluids and postmortem material. Fourth edition. Pharmaceutical Press, London 2011; 1853-1854.
15. Smędra-Kaźmirska A, Żydek L, Barzdo M, Machała W, Berent J. Omyłkowe dożylne podanie roztworu formaliny. Anestezjologia Intensywna Terapia 2009; 41: 163-165.
Artykuł opublikowano w „Archiwum Medycyny Sądowej i Kryminologii” 4/2017.

Źródło:
Archiwum Medycyny Sądowej i Kryminologii/Rafał Skowronek, Małgorzata Korczyńska, Joanna Kulikowska, Joanna Nowicka i Stanisława Kabiesz-Neniczka
Archiwum Medycyny Sądowej i Kryminologii/Rafał Skowronek, Małgorzata Korczyńska, Joanna Kulikowska, Joanna Nowicka i Stanisława Kabiesz-Neniczka



















