Pojawił się genialny lek, który uzdrowi dzieci z zespołem Retta?

Zarejestrowany w USA lek trofinetide to nadzieja dla rodziców – jednak w rozmowie z „Menedżerem Zdrowia” neurolog dziecięca Magdalena Chrościńska-Krawczyk oraz Rafał Janiszewski i Artur Fałek z Kancelarii Doradczej Rafał Piotr Janiszewski są powściągliwi i apelują, by minister zdrowia jak najszybciej zlecił Agencji Oceny Technologii Medycznych i Taryfikacji ekspertyzę.
W marcu 2023 r. Amerykańska Agencja ds. Leków zarejestrowała trofinetide – DAYBUE – w leczeniu pacjentów z zespołem Retta. Czy to nadzieja dla tych osób i czy polskie państwo powinno tę terapię finansować? Zacznijmy od podstaw – pani profesor, co to za choroba?
Magdalena Chrościńska-Krawczyk: – Zespół Retta należy do chorób rzadkich. Występuje z częstością jeden na dziesięć tysięcy. Przede wszystkim u dziewczynek. Spowodowany jest mutacją w genie MECP2, zlokalizowanym na chromosomie X. Gen MECP2 koduje białko MECP2, które jest czynnikiem transkrypcyjnym ulegającym silnej ekspresji w mózgu. Białko to wpływa na różnicowanie i kształtowanie się dendrytów, umożliwia kształtowanie połączeń nerwowych oraz zapobiega apoptozie, czyli zaprogramowanej śmierci neuronów. W przypadku chłopców zespół Retta jest wadą letalną. W całej swojej, niekrótkiej praktyce prowadziłam jednego chłopczyka z tą chorobą. Chłopcy z tym zespołem zwykle umierają w życiu płodowym lub wkrótce po urodzeniu. Natomiast dziewczynki z tą mutacją – która w większości przypadków powstaje de novo, przeważnie na chromosomie pochodzącym od ojca – rodzą się zdrowe. Choroba ujawnia się dopiero po pewnym czasie.
Dziewczynka z zespołem Retta może dostać dziesięć punktów w skali Apgar?
M.Ch.K.: – Jak najbardziej. Okres noworodkowy nie budzi zastrzeżeń ani niepokoju. W typowym przebiegu choroby możemy wyróżnić cztery fazy. Pierwsze nieprawidłowości pojawiają się dopiero – tak jak w wielu chorobach rzadkich – między 6. a 18. miesiącem życia dziecka.
Co wówczas się dzieje?
M.Ch.K.: – Obserwujemy mikrocefalię, czyli małogłowie – główka przestaje rosnąć, oraz słabą aktywność ruchową. Dziecko przestaje osiągać kamienie milowe, to jest konieczne punkty rozwojowe. Bardzo charakterystyczne jest pojawianie się stereotypii ruchowych. Dziewczynki w specyficzny sposób poruszają rączkami. Obserwując właśnie te ruchy, austriacki pediatra i psychiatra Andreas Rett rozpoznał i opisał ten zespół.
Druga faza?
M.Ch.K.: – Między pierwszym a czwartym rokiem życia. To jest najgorszy czas dla tych dzieci, ponieważ dokonuje się szybki regres ich rozwoju. Przede wszystkim rozwoju mowy. Dzieci przestają mówić. Są dziewczynki z zespołem Retta, które w ogóle nie rozwijają mowy, ale większą grupę stanowią te, u których po prawidłowym rozwoju mowy dochodzi do jej regresu. Prócz tego następuje również utrata funkcji motorycznych, w tym umiejętności samodzielnego chodzenia.
Innymi objawami, które w obserwujemy w tej fazie, są hiperwentylacja, bezdechy, zaburzenia snu, cechy autystyczne – czyli „wycofanie” charakterystyczne dla zaburzeń autystycznych, brak interakcji z rówieśnikami – oraz, szczególnie niebezpieczne, napady padaczkowe. O różnej morfologii. To są zarówno napady nieświadomości, jak i uogólnione napady toniczno-kloniczne. Rozpoznajemy padaczkę, często lekooporną, która wymaga włączenia dwóch i więcej leków.
Pojawiają się również zaburzenia wzrastania oraz nadpobudliwość psychoruchowa. Po tych bardzo trudnych latach przychodzi trzecia faza choroby – okres pozornej stabilizacji. Przypada ona na okres przedszkolny i wczesnoszkolny.
Pozorna stabilizacja oznacza poprawę?
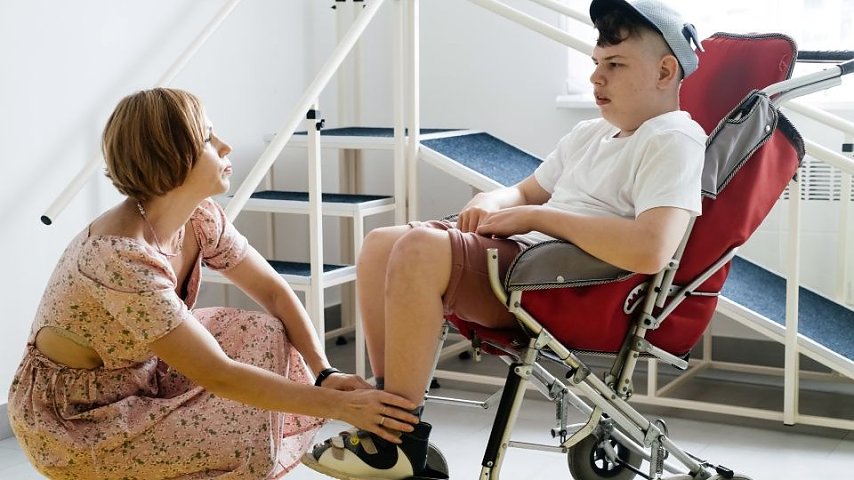
M.Ch.K.: – Dzięki leczeniu i rehabilitacji pojawia się nieznaczna poprawa. Najczęściej, jeśli chodzi o kontakty społeczne. Mniej nasilone są również zaburzenia zachowania i emocji. Niestety, funkcje motoryczne nie polepszają się. Wręcz przeciwnie: powoli, stopniowo następuje dalszy regres. W okresie wczesnoszkolnym większość dziewczynek z zespołem Retta jest już na wózkach inwalidzkich. Obserwujemy wzrost napięcia mięśniowego, ataksję, drżenia mięśniowe. Pojawia się skolioza. Ogromnym problemem pozostają napady padaczkowe, które są trudne do opanowania. Dziewczynki nie rozwijają mowy. Są niepełnosprawne intelektualnie w stopniu od lekkiego po znaczny. Mają małogłowie.
Generalnie zespół Retta jest chorobą uwarunkowaną genetycznie, postępującą, prowadzącą do głębokiej niepełnosprawności, a jednym z największych problemów – z punktu widzenia medycznego – jest towarzysząca tej chorobie padaczka lekooporna.
Jak długo żyją osoby dotknięte tą chorobą?
M.Ch.K.: – Przewidywalna długość życia jest różna i zależy od stopnia zaawansowania choroby. Jednak duża liczba pacjentów z tym zespołem umiera w trzeciej, czwartej dekadzie życia. Od mniej więcej 15. roku życia dziewczynki wchodzą w czwartą i jednocześnie ostatnią fazę choroby, w której następuje poprawa w zakresie kontaktu wzrokowego oraz stabilizacja emocjonalna, jednak nadal występują zaburzenia napadowe, a dalszemu pogorszeniu ulegają funkcje motoryczne. Pojawiają się problemy ortopedyczne – skolioza, deformacje stóp, osteoporoza – oraz problemy gastrologiczne pod postacią refluksu żołądkowo-przełykowego. Pacjentki mają również zaburzenia kardiologiczne, takie jak zaburzenia przewodnictwa przedsionkowo-komorowego oraz wydłużony odstęp Q-T. To właśnie zaburzenia kardiologiczne są najczęstszą przyczyną zgonów dziewcząt i młodych kobiet z zespołem Retta.
Jak leczone są dzieci z zespołem Retta?
M.Ch.K.: – Terapia jest interdyscyplinarna. Przede wszystkim podajemy leki przeciwpadaczkowe oraz stosujemy wszechstronne usprawnianie: fizjoterapię, rehabilitację, terapię zajęciową, zajęcia logopedyczne, z psychologiem, z pedagogiem. Dzieci są również objęte opieką ortopedyczną – gdyż z uwagi na skoliozę wymagają często zabiegów operacyjnych – oraz kardiologiczną.
Mówi pani profesor o leczeniu objawowym…
M.Ch.K.: – W zespole Retta nie ma dostępnego leczenia przyczynowego. Prowadzono badania – i były one dość zaawansowane – z terapią genową…
To pani pierwsza w Polsce leczy terapią genową dzieci z SMA.
M.Ch.K.: – Niestety, dla dzieci z zespołem Retta takiej terapii nie ma. Badania nad terapią genową nie przyniosły jednak zadowalających rezultatów. Obecnie możemy tym dzieciom zaoferować wyłącznie leczenie objawowe, a nie przyczynowe.
Rafał Janiszewski: – To dlatego zarówno środowisko medyczne, jak i oczywiście rodzice chorych dzieci wyczekują z niecierpliwością nowej technologii, która powodowałaby wyleczenie. I jeśli tylko na świecie pojawia się coś, o czym mówi się, że może proces chorobowy spowolnić, patrzą na to z ogromną nadzieją. To jest całkowicie zrozumiałe, że wobec dramatycznej sytuacji dzieci ich rodzice oraz terapeuci oczekują nowej technologii tak bardzo, że to pragnienie potrafi czasem przesłonić racjonalne spojrzenie.
W medycynie często mamy sytuację, że na nieuleczalne choroby, które jesteśmy w stanie leczyć wyłącznie objawowo, pojawia się „supertechnologia z kosmosu” z opisem „woda namagnesowana siłami wszechświata”. I niektórzy pacjenci oraz ich rodziny tych paramedycznych metod się chwytają. I wszystkiego, czego mogą się chwycić. Bo to im daje nadzieję. My natomiast jesteśmy fachowcami i musimy się opierać na faktach! Dowodach naukowych.
Rozmawiamy nie o „technologii z kosmosu”, ale o zarejestrowanym w USA leku trofinetide.
Artur Fałek: – Świat jest mały, dlatego ta technologia lada moment trafi do Europy. Jest tylko kwestią czasu, kiedy zostanie dopuszczona do obrotu przez Europejską Agencję Leków.
Co to za lek? Jak on działa?
M.Ch.K.: – Do końca nie wiemy, jak on działa. O to właśnie chodzi.
A.F.: – To jest technologia, której mechanizm do końca nie jest znany i niedosyt wiedzy w tym zakresie jest dużym problemem nie tylko dla lekarzy, ale i dla regulatora. Doświadczenia kliniczne są takie, że pacjenci uzyskali poprawę stanu zdrowia mierzonego kwestionariuszem oceniającym ich sprawność. Dostępne dane są jednak bardzo ogólne. Mamy do czynienia z chorobą, która nieuchronnie prowadzi do śmierci – i to w młodym wieku. Czego w takiej sytuacji oczekujemy? Terapii, która rozwiązuje problem w sposób radykalny! Terapii, której zastosowanie spowoduje, że pacjent będzie żył tak długo, jak przewiduje się średnią długość życia w populacji.
Mówiąc krótko – przełomowa terapia powinna pacjentki wyleczyć.
A.F.: – Właśnie tak. Natomiast trofinetide nie daje efektu wyleczenia. W badaniach potwierdzono jedynie poprawę stanu klinicznego. Jak dużą? Dopiero wieloletnie stosowanie tej terapii da nam na to odpowiedź, dlatego że czym innym jest badanie kliniczne, a czym innym zastosowanie leku w populacji ogólnej, czyli we wskazaniach rejestracyjnych. Pytanie, czy wówczas lek przyniesie taki sam efekt jak w badaniu klinicznym.
R.J.: – Możemy tę technologię oceniać na zimno. Minister zdrowia może, a nawet musi, ją oceniać też w taki sposób, by zdecydować, czy państwo jest w stanie tę technologię finansować. Jednak na ministrze zdrowia świat się nie kończy. Kluczowy jest lekarz, do którego przychodzi zdesperowany rodzic. Medyk znajduje się pod bardzo silną presją. Ogromne jest bowiem oczekiwanie rodziców, że lekarz ten lek zastosuje.
To naturalna reakcja, że rodzice powiedzą: „Pani profesor, chcemy zastosować u naszego dziecka ten amerykański lek”.
M.Ch.K.: – Jak najbardziej rozumiem tych rodziców. Jeśli pojawiło się chociażby małe światełko dające nadzieję na to, że spowolnimy rozwój choroby, to uważają, że gra jest warta świeczki. Jednak jest małe „ale” – nie znamy dokładnego mechanizmu działania tego leku. Jest powiedziane, że prawdopodobnie polega on na stymulowaniu dojrzewania synaptycznego, dojrzewania komórek nerwowych. Ma również działanie przeciwzapalne. Podkreślam – prawdopodobnie. Po drugie wiemy, że ten lek nie jest pozbawiony działań niepożądanych. Pojawiają się biegunka, wymioty, spadek masy ciała, są działania niepożądane pod postacią drgawek, czyli napadów padaczkowych. Opisywanych jest dziewięć procent takich skutków ubocznych. Co jeszcze mnie niepokoi? To, że mam za mało danych mówiących o tym, co tak naprawdę się poprawiło u stosujących ten lek dzieci. Wiemy, że troszkę się polepszyło ich funkcjonowanie ruchowe. Czy jednak zredukowała się liczba napadów padaczkowych? Czy poprawiło się ich funkcjonowanie intelektualne? Na ile stosowanie leku zahamowało postęp choroby? Trudno powiedzieć.
Podkreślam – doskonale rozumiem rodziców. Sama walczyłabym jak lwica o swoje dziecko. Wiem, że rodzice będą błagać, by ten lek sprowadzić z USA i podać go ich dzieciom.
R.J.: – A plotki z rynku są takie, że roczny koszt leczenia będzie sięgał miliona złotych. Czy minister zdrowia podejmie się finansowania leku, którego mechanizmu działania do końca nie znamy – sam producent go nie zna… To nie chodzi o to, że „nie wiemy, jak to działa, ale działa”. To by było pół biedy. W znajomości mechanizmu działania leku najistotniejsze jest to, że jeśliby po jego podaniu z pacjentem działo się coś złego, to wiedzielibyśmy, czym to jest spowodowane. A w tym przypadku tego nie wiemy. To jest jedna rzecz.
Druga jest taka, że minister będzie oczywiście patrzył na to, jaką korzyść kliniczną uzyska pacjent. I nie będzie widział oczami rodziców, będących są w stanie za milion złotych kupić chociażby nadzieję. Minister będzie chciał odpowiedzi na pytanie, czy za ten milion złotych kupi rzeczywistą poprawę stanu zdrowia dzieci.
Jeśli refundacji nie będzie, to nietrudno przewidzieć, co się wydarzy: rozpoczną się zbiórki w internecie.
R.J. i M.Ch.K.: – Rodzice już zbierają pieniądze.
R.J.: – A ja myślę o tym, w jakiej sytuacji wobec tego znajduje się pani, której wiedza i doświadczenie podpowiadają, że nie może do tego podejść „na hurra”, a jednocześnie ma do czynienia z ogromnym oczekiwaniem rodziców, że ich dziecko dostanie ten lek. Dotychczas w ogóle pomijaliśmy aspekt finansowy, a on jest przecież – delikatnie mówiąc – niebagatelny. Dlatego chciałbym postawić tezę, że jeżeli pojawia się nowa technologia, to powinna mieć regulacje – przynajmniej europejskie – co do ceny. Bo zobaczmy, co tak naprawdę teraz się dzieje. Pojawia się technologia, która - jak wynika z literatury naukowej - wcale nie jest przełomowa, a cena jest ogromna. Milion złotych za nadzieję. Czy na poziomie Unii Europejskiej nie powinniśmy zapobiegać takim sytuacjom? I jeszcze jedna rzecz – jestem za tym, by otoczyć parasolem ochronnym wszystkie chore dzieci.
Dziś pytam jednak również o to, kto i jakimi narzędziami uchroni terapeutę przed tak potężnym dylematem, przed jakim stoi dzisiaj między innymi pani, lecząca dzieci z zespołem Retta, gdy po uzbieraniu miliona przychodzą do niej rodzice i mówią: „Sprowadźmy ten lek, niech go pani poda”.
A.F.: – Zawsze powtarzam, że na tym świecie nic prócz miłości rodzicielskiej nie jest za darmo. Niestety, leki kosztują. Jest to towar, który ktoś wytwarza – a po to, żeby go wyprodukować, musi zainwestować czas i pieniądze w badania naukowe oraz proces technologiczny. I trzeba za to zapłacić. Natomiast kluczowe pytanie brzmi: ile leki mogą kosztować.
R.J.: – Powiem prosto z serca – według mnie cena tego leku to bandytyzm. Rozbój. W przypadku SMA mieliśmy bardzo zaawansowaną technologię, gdzie koszty badań naukowych, eksperymentów były ogromne, dlatego rozumiem, że podmiot odpowiedzialny zażyczył sobie za terapię genową kilka milionów. Chociaż wolałbym, żeby zażądał mniej. Natomiast w przypadku trofinetide nie mamy do czynienia z zaawansowaną technologią. Mamy do czynienia z normalną substancją chemiczną. Dlatego uważam, że tak wysoka cena jest niewspółmierna do niczego. Jest to żerowanie na dramatycznej sytuacji tych dzieci. Wykorzystywanie rozpaczy ich rodziców.
A.F.: – Zgadzam się z twoją opinią.
A czy pani również jest tego zdania?
M.Ch.K.: – Jak najbardziej tak.
A.F.: – Spójrzmy na wzór strukturalny trójpeptydu, z którego składa się ten lek! To nie jest skomplikowana cząsteczka, zatem koszt jego wytwarzania nie jest duży. Rozumiem – koszty badań. Rozumiem – choroba rzadka. Wszystko jednak powinno mieć granice. A granicą, prócz przyzwoitości, są również zdolności systemu ochrony zdrowia. Cena, o której dziś rozmawiamy, czyli milion złotych za roczną terapię, przekracza możliwości finansowe rodzin tych dzieci. A pamiętajmy, że nie rozmawiamy o rocznej terapii – mamy perspektywę kilkudziesięciu lat, kiedy należałoby tę terapię stosować. Nie wiemy, czy ona przedłuża życie…
M.Ch.K.: – Ani o ile…
A.F.: – Punkty końcowe są tak określone, że całe badanie było ukierunkowane na tę ankietę. Nie wiemy, czy nie wychodziły inne punkty końcowe, czy po prostu możliwość ich zbadania była ograniczona. Te badania przeprowadzono na dość niewielkiej populacji.
M.Ch.K.: – Dokładnie na 187 pacjentkach.
A.F.: – Patrząc na statystyki w samym województwie lubelskim, znaleźlibyśmy tyle pacjentek. Możliwość przeprowadzenia badań na szerszej populacji istnieje i mam nadzieję, że takie badania będą prowadzone w systemie sieciowym, to znaczy ośrodki prowadzące terapie tym lekiem będą się wymieniały doświadczeniami. Natomiast sytuacja, w jakiej się znaleźliśmy, skłania nas do tego, o czym mówi Rafał – do patrzenia ponadpaństwowego, przez pryzmat całej Europy. Od kilkunastu lat trwają rozmowy o równym dostępie do zdrowia na poziomie europejskim.
R.J.: – Mówisz o pricingu, a ja jestem bardziej radykalny. Uważam, że jeśli ktoś ma dopuszczać do obrotu technologię medyczną – gdy rozmawiamy o obszarze szczególnie regulowanym – to przed zarejestrowaniem leku oczywiście należy sprawdzić wartość kliniczną i bezpieczeństwo, a następnie zapytać podmiot, ile on za to chce. Bo jeśli będzie chciał milion, a według nas to nie jest tego warte, to mu tego nie wpuścimy na rynek. Pomimo swobody handlu i działalności gospodarczej. Medycyna to nie jest swobodna działalność gospodarcza. To jest odpowiedzialność za ludzi. Nawet jeśli nie będziemy refundować tego leku, to jest rzeczą oczywistą, że obywatele będą zbierać na niego pieniądze, a potem dziecku podawać. Rodzice dzieci z zespołem Retta zgłaszają się do mojej kancelarii doradczej.
Jak wielu?
R.J.: – Bardzo dużo osób. Moim zdaniem już dzisiaj firma farmaceutyczna ma gotowy pakiet zamówień z całego świata. Ci rodzice kupią nawet za milion. A jeśli ich dzieciom to nie pomoże, jeśli zaszkodzi, to kto poniesie tego konsekwencje?
M.Ch.K.: – Ten, kto prowadzi terapię! Lekarz…
R.J.: – W rzeczy samej.
M.Ch.K.: – Ponieważ lekarz powiedział: „Dobrze, zgadzam się, podam dziecku ten lek i biorę za to pełną odpowiedzialność”. Za ewentualne wystąpienie działań niepożądanych i wszelkie nieprzewidywalne sytuacje również. Nie bierze za to odpowiedzialności producent leku, tylko lekarz, który danemu pacjentowi w konkretnym szpitalu ten lek poda.Tak samo było wtedy, kiedy w Uniwersyteckim Szpitalu Dziecięcym w Lublinie wzięliśmy trzy lata temu odpowiedzialność za podanie terapii genowej dzieciom z SMA.
Poza panią nikt w Polsce na to wówczas się nie zdecydował.
M.Ch.K.: – Zolgensmę dostało u nas 46 pacjentów.
Zapytam wprost – nie będzie pani podawała trofinetide dzieciom z zespołem Retta?
M.Ch.K.: – Nie będę, dopóki nie będę miała wystarczających danych dotyczących tego leku. W przypadku terapii genowej w leczeniu SMA wiedziałam wszystko: jakich efektów możemy się spodziewać, jakie mogą wystąpić działania niepożądane, jaki jest dokładny mechanizm działania. W tym przypadku mam natomiast jakiś lek, którego mechanizmu działania do końca nie znam. Równie dobrze może być on taki sam jak zwykłego pirocetamu – neuroprotekcyjne działanie ochronne na ośrodkowy układ nerwowy. Pirocetam można kupić w każdej aptece za grosze, a nie za miliony. Co nie zmienia faktu, że wiem, że jeśli nie zrobimy tego w Polsce, to ci rodzice pojadą z dziećmi do Stanów Zjednoczonych, co oznacza, że poniosą dodatkowe koszty związane z lotem i zakwaterowaniem.
R.J.: – Rodzice pojadą do USA, ponieważ nie analizują tej sytuacji w taki sposób, jak my ją analizujemy.
A.F.: – Mają pieniądze na rok, dwa czy trzy lata terapii? Pewnie nie będzie ich stać na kilkadziesiąt podań. Pytanie, co potem?
R.J.: – Gdy rozmawiam z rodzicami, to mówią: „Na rok uzbieraliśmy i zobaczymy, czy będzie działać, bo jeśli nie, to przestaniemy podawać ten lek”. A ja pytam: A co wiemy na temat przerwania terapii? Otóż nic o tym nie wiemy.
M.Ch.K.: – A co wiemy na temat długoterminowego stosowania terapii? Również nic.
Pani nie rekomenduje rodzicom podawania tego leku. Co w tej sytuacji ma zrobić minister zdrowia?
A.F.: – Mamy całkiem niezłą procedurę podejmowania decyzji refundacyjnej. Minister nie ma wpływu na to, czy zostanie złożony wniosek refundacyjny, czy nie – chociaż uważam, że to nie jest do końca w porządku, bo jeżeli się pojawia nowa technologia, to złożenie wniosku powinno być obowiązkiem podmiotu odpowiedzialnego. Jeśli zostanie złożony, to rozpoczyna się procedura oceny. I wchodzi do gry Agencja Oceny Technologii Medycznych i Taryfikacji. Ona na te wszystkie wątpliwości, o których dziś mówiliśmy – czyli dotyczące jakości materiału dowodowego, jakości badań klinicznych wziętych pod uwagę przy rejestracji – popatrzy pod kątem refundacji.
Zawsze podkreślam, że procedury rejestracyjne różnią się od refundacyjnych, bo czym innym jest dopuszczenie do obrotu i stworzenie warunków do zbadania, jak lek działa, gdy się go używa zgodnie ze wskazaniami rejestracyjnymi, a czym innym jest decyzja o tym, żeby wydawać na coś pieniądze publiczne.
R.J.: – I to jest świetna konkluzja. Wniosek mój jest taki, że minister zdrowia powinien skierować tę technologię do oceny przez AOTMiT. A agencja oceniłaby jej wartość kliniczną i finansową, po czym wszem i wobec opublikowałaby swój raport. I to zarówno w języku dla terapeutów, jak i dla rodziców. Byłoby to wyrażeniem przez ministra troski o chore dzieci, których rodzicom dziś przychodzi do głowy, żeby pojechać od Stanów Zjednoczonych.
Szef resortu zdrowia jest przecież również od tego, by obywateli informować, budować świadomość, zapobiegać ryzykom i niebezpieczeństwom. Ma ku temu instrumenty.
M.Ch.K.: – W ten sposób minister otoczyłby opieką nie tylko rodziców, ale też lekarzy chcących tę technologię zastosować. Nie zostawiałby ich dłużej samych na zasadzie: „Róbcie sobie, co chcecie, a potem to wy bierzcie za to odpowiedzialność”.
A.F.: – Autorytet regulatora powinien być w tej sytuacji dobrze wykorzystany. Skierowanie do AOTMiT powinno się pojawić przy pierwszym wniosku o zrefundowanie leku w imporcie docelowym.
M.Ch.K.: – Powiem przewrotnie – jeśli to miałoby ministra do tego skłonić, mogę taki wniosek napisać.
A.F.: – Konkludując: rozmawialiśmy również o idei europejskiego zdrowia i warto zwrócić uwagę, że mamy przykłady udanej współpracy państw członkowskich…
Na poziomie unijnym negocjowano ceny szczepionek przeciwko COVID-19.
A.F.: – Otóż to. A zatem ewentualność prowadzenia negocjacji i ustalania cen na poziomie europejskim istnieje. I wydaje mi się, że powinna być wykorzystywana częściej.
R.J.: – Chodzi wszak o zapobieganie rozbójniczemu działaniu na rynku leków. A na już rekomendujemy – niech AOTMiT oceni trofinetide. Rodzice w całej Europie wypatrują, czy lek zostanie zarejestrowany również u nas. A kiedy to się stanie, to wydarzy się to samo, co w USA – pojawią się nagłówki: „Jest lek na zespół Retta”. Co jest nieprawdą.
M.Ch.K.: – Nieprawdą.
R.J.: – Tym bardziej minister zdrowia powinien działać teraz. Zanim lek zostanie zarejestrowany. Agencja powinna mieć już w ręku raport i ogłosić, jak ocenia ten lek. Ja go nie dyskryminuję. Może w jakiś sposób działa, jednak moim zdaniem nie jest wart miliona i informacja medialna, jaka się w związku z nim pojawiła, jest nieprawdziwa.
Dla rodziców chorych dzieci najistotniejsze jest poczucie, że robią dla nich wszystko, co najlepsze. Pani profesor, proszę – jako autorytet – powiedzieć, czy nie zbierając miliona złotych na nowy lek, mogą mieć takie poczucie?
M.Ch.K.: – Według mnie zdecydowanie tak. Z pełną odpowiedzialnością mogę powiedzieć, że nie znamy do końca mechanizmu działania tego leku, badania są zbyt mało precyzyjne i przeprowadzono je na zbyt małej grupie chorych. Dopóki nie będziemy mieli więcej danych, podchodziłabym do leczenia tym lekiem bardzo ostrożnie.

Magdalena Chrościńska-Krawczyk: – Zespół Retta należy do chorób rzadkich. Występuje z częstością jeden na dziesięć tysięcy. Przede wszystkim u dziewczynek. Spowodowany jest mutacją w genie MECP2, zlokalizowanym na chromosomie X. Gen MECP2 koduje białko MECP2, które jest czynnikiem transkrypcyjnym ulegającym silnej ekspresji w mózgu. Białko to wpływa na różnicowanie i kształtowanie się dendrytów, umożliwia kształtowanie połączeń nerwowych oraz zapobiega apoptozie, czyli zaprogramowanej śmierci neuronów. W przypadku chłopców zespół Retta jest wadą letalną. W całej swojej, niekrótkiej praktyce prowadziłam jednego chłopczyka z tą chorobą. Chłopcy z tym zespołem zwykle umierają w życiu płodowym lub wkrótce po urodzeniu. Natomiast dziewczynki z tą mutacją – która w większości przypadków powstaje de novo, przeważnie na chromosomie pochodzącym od ojca – rodzą się zdrowe. Choroba ujawnia się dopiero po pewnym czasie.
Dziewczynka z zespołem Retta może dostać dziesięć punktów w skali Apgar?
M.Ch.K.: – Jak najbardziej. Okres noworodkowy nie budzi zastrzeżeń ani niepokoju. W typowym przebiegu choroby możemy wyróżnić cztery fazy. Pierwsze nieprawidłowości pojawiają się dopiero – tak jak w wielu chorobach rzadkich – między 6. a 18. miesiącem życia dziecka.
Co wówczas się dzieje?
M.Ch.K.: – Obserwujemy mikrocefalię, czyli małogłowie – główka przestaje rosnąć, oraz słabą aktywność ruchową. Dziecko przestaje osiągać kamienie milowe, to jest konieczne punkty rozwojowe. Bardzo charakterystyczne jest pojawianie się stereotypii ruchowych. Dziewczynki w specyficzny sposób poruszają rączkami. Obserwując właśnie te ruchy, austriacki pediatra i psychiatra Andreas Rett rozpoznał i opisał ten zespół.
Druga faza?
M.Ch.K.: – Między pierwszym a czwartym rokiem życia. To jest najgorszy czas dla tych dzieci, ponieważ dokonuje się szybki regres ich rozwoju. Przede wszystkim rozwoju mowy. Dzieci przestają mówić. Są dziewczynki z zespołem Retta, które w ogóle nie rozwijają mowy, ale większą grupę stanowią te, u których po prawidłowym rozwoju mowy dochodzi do jej regresu. Prócz tego następuje również utrata funkcji motorycznych, w tym umiejętności samodzielnego chodzenia.
Innymi objawami, które w obserwujemy w tej fazie, są hiperwentylacja, bezdechy, zaburzenia snu, cechy autystyczne – czyli „wycofanie” charakterystyczne dla zaburzeń autystycznych, brak interakcji z rówieśnikami – oraz, szczególnie niebezpieczne, napady padaczkowe. O różnej morfologii. To są zarówno napady nieświadomości, jak i uogólnione napady toniczno-kloniczne. Rozpoznajemy padaczkę, często lekooporną, która wymaga włączenia dwóch i więcej leków.
Pojawiają się również zaburzenia wzrastania oraz nadpobudliwość psychoruchowa. Po tych bardzo trudnych latach przychodzi trzecia faza choroby – okres pozornej stabilizacji. Przypada ona na okres przedszkolny i wczesnoszkolny.
Pozorna stabilizacja oznacza poprawę?
M.Ch.K.: – Dzięki leczeniu i rehabilitacji pojawia się nieznaczna poprawa. Najczęściej, jeśli chodzi o kontakty społeczne. Mniej nasilone są również zaburzenia zachowania i emocji. Niestety, funkcje motoryczne nie polepszają się. Wręcz przeciwnie: powoli, stopniowo następuje dalszy regres. W okresie wczesnoszkolnym większość dziewczynek z zespołem Retta jest już na wózkach inwalidzkich. Obserwujemy wzrost napięcia mięśniowego, ataksję, drżenia mięśniowe. Pojawia się skolioza. Ogromnym problemem pozostają napady padaczkowe, które są trudne do opanowania. Dziewczynki nie rozwijają mowy. Są niepełnosprawne intelektualnie w stopniu od lekkiego po znaczny. Mają małogłowie.
Generalnie zespół Retta jest chorobą uwarunkowaną genetycznie, postępującą, prowadzącą do głębokiej niepełnosprawności, a jednym z największych problemów – z punktu widzenia medycznego – jest towarzysząca tej chorobie padaczka lekooporna.
Jak długo żyją osoby dotknięte tą chorobą?
M.Ch.K.: – Przewidywalna długość życia jest różna i zależy od stopnia zaawansowania choroby. Jednak duża liczba pacjentów z tym zespołem umiera w trzeciej, czwartej dekadzie życia. Od mniej więcej 15. roku życia dziewczynki wchodzą w czwartą i jednocześnie ostatnią fazę choroby, w której następuje poprawa w zakresie kontaktu wzrokowego oraz stabilizacja emocjonalna, jednak nadal występują zaburzenia napadowe, a dalszemu pogorszeniu ulegają funkcje motoryczne. Pojawiają się problemy ortopedyczne – skolioza, deformacje stóp, osteoporoza – oraz problemy gastrologiczne pod postacią refluksu żołądkowo-przełykowego. Pacjentki mają również zaburzenia kardiologiczne, takie jak zaburzenia przewodnictwa przedsionkowo-komorowego oraz wydłużony odstęp Q-T. To właśnie zaburzenia kardiologiczne są najczęstszą przyczyną zgonów dziewcząt i młodych kobiet z zespołem Retta.
Jak leczone są dzieci z zespołem Retta?
M.Ch.K.: – Terapia jest interdyscyplinarna. Przede wszystkim podajemy leki przeciwpadaczkowe oraz stosujemy wszechstronne usprawnianie: fizjoterapię, rehabilitację, terapię zajęciową, zajęcia logopedyczne, z psychologiem, z pedagogiem. Dzieci są również objęte opieką ortopedyczną – gdyż z uwagi na skoliozę wymagają często zabiegów operacyjnych – oraz kardiologiczną.
Mówi pani profesor o leczeniu objawowym…
M.Ch.K.: – W zespole Retta nie ma dostępnego leczenia przyczynowego. Prowadzono badania – i były one dość zaawansowane – z terapią genową…
To pani pierwsza w Polsce leczy terapią genową dzieci z SMA.
M.Ch.K.: – Niestety, dla dzieci z zespołem Retta takiej terapii nie ma. Badania nad terapią genową nie przyniosły jednak zadowalających rezultatów. Obecnie możemy tym dzieciom zaoferować wyłącznie leczenie objawowe, a nie przyczynowe.
Rafał Janiszewski: – To dlatego zarówno środowisko medyczne, jak i oczywiście rodzice chorych dzieci wyczekują z niecierpliwością nowej technologii, która powodowałaby wyleczenie. I jeśli tylko na świecie pojawia się coś, o czym mówi się, że może proces chorobowy spowolnić, patrzą na to z ogromną nadzieją. To jest całkowicie zrozumiałe, że wobec dramatycznej sytuacji dzieci ich rodzice oraz terapeuci oczekują nowej technologii tak bardzo, że to pragnienie potrafi czasem przesłonić racjonalne spojrzenie.
W medycynie często mamy sytuację, że na nieuleczalne choroby, które jesteśmy w stanie leczyć wyłącznie objawowo, pojawia się „supertechnologia z kosmosu” z opisem „woda namagnesowana siłami wszechświata”. I niektórzy pacjenci oraz ich rodziny tych paramedycznych metod się chwytają. I wszystkiego, czego mogą się chwycić. Bo to im daje nadzieję. My natomiast jesteśmy fachowcami i musimy się opierać na faktach! Dowodach naukowych.
Rozmawiamy nie o „technologii z kosmosu”, ale o zarejestrowanym w USA leku trofinetide.
Artur Fałek: – Świat jest mały, dlatego ta technologia lada moment trafi do Europy. Jest tylko kwestią czasu, kiedy zostanie dopuszczona do obrotu przez Europejską Agencję Leków.
Co to za lek? Jak on działa?
M.Ch.K.: – Do końca nie wiemy, jak on działa. O to właśnie chodzi.
A.F.: – To jest technologia, której mechanizm do końca nie jest znany i niedosyt wiedzy w tym zakresie jest dużym problemem nie tylko dla lekarzy, ale i dla regulatora. Doświadczenia kliniczne są takie, że pacjenci uzyskali poprawę stanu zdrowia mierzonego kwestionariuszem oceniającym ich sprawność. Dostępne dane są jednak bardzo ogólne. Mamy do czynienia z chorobą, która nieuchronnie prowadzi do śmierci – i to w młodym wieku. Czego w takiej sytuacji oczekujemy? Terapii, która rozwiązuje problem w sposób radykalny! Terapii, której zastosowanie spowoduje, że pacjent będzie żył tak długo, jak przewiduje się średnią długość życia w populacji.
Mówiąc krótko – przełomowa terapia powinna pacjentki wyleczyć.
A.F.: – Właśnie tak. Natomiast trofinetide nie daje efektu wyleczenia. W badaniach potwierdzono jedynie poprawę stanu klinicznego. Jak dużą? Dopiero wieloletnie stosowanie tej terapii da nam na to odpowiedź, dlatego że czym innym jest badanie kliniczne, a czym innym zastosowanie leku w populacji ogólnej, czyli we wskazaniach rejestracyjnych. Pytanie, czy wówczas lek przyniesie taki sam efekt jak w badaniu klinicznym.
R.J.: – Możemy tę technologię oceniać na zimno. Minister zdrowia może, a nawet musi, ją oceniać też w taki sposób, by zdecydować, czy państwo jest w stanie tę technologię finansować. Jednak na ministrze zdrowia świat się nie kończy. Kluczowy jest lekarz, do którego przychodzi zdesperowany rodzic. Medyk znajduje się pod bardzo silną presją. Ogromne jest bowiem oczekiwanie rodziców, że lekarz ten lek zastosuje.
To naturalna reakcja, że rodzice powiedzą: „Pani profesor, chcemy zastosować u naszego dziecka ten amerykański lek”.
M.Ch.K.: – Jak najbardziej rozumiem tych rodziców. Jeśli pojawiło się chociażby małe światełko dające nadzieję na to, że spowolnimy rozwój choroby, to uważają, że gra jest warta świeczki. Jednak jest małe „ale” – nie znamy dokładnego mechanizmu działania tego leku. Jest powiedziane, że prawdopodobnie polega on na stymulowaniu dojrzewania synaptycznego, dojrzewania komórek nerwowych. Ma również działanie przeciwzapalne. Podkreślam – prawdopodobnie. Po drugie wiemy, że ten lek nie jest pozbawiony działań niepożądanych. Pojawiają się biegunka, wymioty, spadek masy ciała, są działania niepożądane pod postacią drgawek, czyli napadów padaczkowych. Opisywanych jest dziewięć procent takich skutków ubocznych. Co jeszcze mnie niepokoi? To, że mam za mało danych mówiących o tym, co tak naprawdę się poprawiło u stosujących ten lek dzieci. Wiemy, że troszkę się polepszyło ich funkcjonowanie ruchowe. Czy jednak zredukowała się liczba napadów padaczkowych? Czy poprawiło się ich funkcjonowanie intelektualne? Na ile stosowanie leku zahamowało postęp choroby? Trudno powiedzieć.
Podkreślam – doskonale rozumiem rodziców. Sama walczyłabym jak lwica o swoje dziecko. Wiem, że rodzice będą błagać, by ten lek sprowadzić z USA i podać go ich dzieciom.
R.J.: – A plotki z rynku są takie, że roczny koszt leczenia będzie sięgał miliona złotych. Czy minister zdrowia podejmie się finansowania leku, którego mechanizmu działania do końca nie znamy – sam producent go nie zna… To nie chodzi o to, że „nie wiemy, jak to działa, ale działa”. To by było pół biedy. W znajomości mechanizmu działania leku najistotniejsze jest to, że jeśliby po jego podaniu z pacjentem działo się coś złego, to wiedzielibyśmy, czym to jest spowodowane. A w tym przypadku tego nie wiemy. To jest jedna rzecz.
Druga jest taka, że minister będzie oczywiście patrzył na to, jaką korzyść kliniczną uzyska pacjent. I nie będzie widział oczami rodziców, będących są w stanie za milion złotych kupić chociażby nadzieję. Minister będzie chciał odpowiedzi na pytanie, czy za ten milion złotych kupi rzeczywistą poprawę stanu zdrowia dzieci.
Jeśli refundacji nie będzie, to nietrudno przewidzieć, co się wydarzy: rozpoczną się zbiórki w internecie.
R.J. i M.Ch.K.: – Rodzice już zbierają pieniądze.
R.J.: – A ja myślę o tym, w jakiej sytuacji wobec tego znajduje się pani, której wiedza i doświadczenie podpowiadają, że nie może do tego podejść „na hurra”, a jednocześnie ma do czynienia z ogromnym oczekiwaniem rodziców, że ich dziecko dostanie ten lek. Dotychczas w ogóle pomijaliśmy aspekt finansowy, a on jest przecież – delikatnie mówiąc – niebagatelny. Dlatego chciałbym postawić tezę, że jeżeli pojawia się nowa technologia, to powinna mieć regulacje – przynajmniej europejskie – co do ceny. Bo zobaczmy, co tak naprawdę teraz się dzieje. Pojawia się technologia, która - jak wynika z literatury naukowej - wcale nie jest przełomowa, a cena jest ogromna. Milion złotych za nadzieję. Czy na poziomie Unii Europejskiej nie powinniśmy zapobiegać takim sytuacjom? I jeszcze jedna rzecz – jestem za tym, by otoczyć parasolem ochronnym wszystkie chore dzieci.
Dziś pytam jednak również o to, kto i jakimi narzędziami uchroni terapeutę przed tak potężnym dylematem, przed jakim stoi dzisiaj między innymi pani, lecząca dzieci z zespołem Retta, gdy po uzbieraniu miliona przychodzą do niej rodzice i mówią: „Sprowadźmy ten lek, niech go pani poda”.
A.F.: – Zawsze powtarzam, że na tym świecie nic prócz miłości rodzicielskiej nie jest za darmo. Niestety, leki kosztują. Jest to towar, który ktoś wytwarza – a po to, żeby go wyprodukować, musi zainwestować czas i pieniądze w badania naukowe oraz proces technologiczny. I trzeba za to zapłacić. Natomiast kluczowe pytanie brzmi: ile leki mogą kosztować.
R.J.: – Powiem prosto z serca – według mnie cena tego leku to bandytyzm. Rozbój. W przypadku SMA mieliśmy bardzo zaawansowaną technologię, gdzie koszty badań naukowych, eksperymentów były ogromne, dlatego rozumiem, że podmiot odpowiedzialny zażyczył sobie za terapię genową kilka milionów. Chociaż wolałbym, żeby zażądał mniej. Natomiast w przypadku trofinetide nie mamy do czynienia z zaawansowaną technologią. Mamy do czynienia z normalną substancją chemiczną. Dlatego uważam, że tak wysoka cena jest niewspółmierna do niczego. Jest to żerowanie na dramatycznej sytuacji tych dzieci. Wykorzystywanie rozpaczy ich rodziców.
A.F.: – Zgadzam się z twoją opinią.
A czy pani również jest tego zdania?
M.Ch.K.: – Jak najbardziej tak.
A.F.: – Spójrzmy na wzór strukturalny trójpeptydu, z którego składa się ten lek! To nie jest skomplikowana cząsteczka, zatem koszt jego wytwarzania nie jest duży. Rozumiem – koszty badań. Rozumiem – choroba rzadka. Wszystko jednak powinno mieć granice. A granicą, prócz przyzwoitości, są również zdolności systemu ochrony zdrowia. Cena, o której dziś rozmawiamy, czyli milion złotych za roczną terapię, przekracza możliwości finansowe rodzin tych dzieci. A pamiętajmy, że nie rozmawiamy o rocznej terapii – mamy perspektywę kilkudziesięciu lat, kiedy należałoby tę terapię stosować. Nie wiemy, czy ona przedłuża życie…
M.Ch.K.: – Ani o ile…
A.F.: – Punkty końcowe są tak określone, że całe badanie było ukierunkowane na tę ankietę. Nie wiemy, czy nie wychodziły inne punkty końcowe, czy po prostu możliwość ich zbadania była ograniczona. Te badania przeprowadzono na dość niewielkiej populacji.
M.Ch.K.: – Dokładnie na 187 pacjentkach.
A.F.: – Patrząc na statystyki w samym województwie lubelskim, znaleźlibyśmy tyle pacjentek. Możliwość przeprowadzenia badań na szerszej populacji istnieje i mam nadzieję, że takie badania będą prowadzone w systemie sieciowym, to znaczy ośrodki prowadzące terapie tym lekiem będą się wymieniały doświadczeniami. Natomiast sytuacja, w jakiej się znaleźliśmy, skłania nas do tego, o czym mówi Rafał – do patrzenia ponadpaństwowego, przez pryzmat całej Europy. Od kilkunastu lat trwają rozmowy o równym dostępie do zdrowia na poziomie europejskim.
R.J.: – Mówisz o pricingu, a ja jestem bardziej radykalny. Uważam, że jeśli ktoś ma dopuszczać do obrotu technologię medyczną – gdy rozmawiamy o obszarze szczególnie regulowanym – to przed zarejestrowaniem leku oczywiście należy sprawdzić wartość kliniczną i bezpieczeństwo, a następnie zapytać podmiot, ile on za to chce. Bo jeśli będzie chciał milion, a według nas to nie jest tego warte, to mu tego nie wpuścimy na rynek. Pomimo swobody handlu i działalności gospodarczej. Medycyna to nie jest swobodna działalność gospodarcza. To jest odpowiedzialność za ludzi. Nawet jeśli nie będziemy refundować tego leku, to jest rzeczą oczywistą, że obywatele będą zbierać na niego pieniądze, a potem dziecku podawać. Rodzice dzieci z zespołem Retta zgłaszają się do mojej kancelarii doradczej.
Jak wielu?
R.J.: – Bardzo dużo osób. Moim zdaniem już dzisiaj firma farmaceutyczna ma gotowy pakiet zamówień z całego świata. Ci rodzice kupią nawet za milion. A jeśli ich dzieciom to nie pomoże, jeśli zaszkodzi, to kto poniesie tego konsekwencje?
M.Ch.K.: – Ten, kto prowadzi terapię! Lekarz…
R.J.: – W rzeczy samej.
M.Ch.K.: – Ponieważ lekarz powiedział: „Dobrze, zgadzam się, podam dziecku ten lek i biorę za to pełną odpowiedzialność”. Za ewentualne wystąpienie działań niepożądanych i wszelkie nieprzewidywalne sytuacje również. Nie bierze za to odpowiedzialności producent leku, tylko lekarz, który danemu pacjentowi w konkretnym szpitalu ten lek poda.Tak samo było wtedy, kiedy w Uniwersyteckim Szpitalu Dziecięcym w Lublinie wzięliśmy trzy lata temu odpowiedzialność za podanie terapii genowej dzieciom z SMA.
Poza panią nikt w Polsce na to wówczas się nie zdecydował.
M.Ch.K.: – Zolgensmę dostało u nas 46 pacjentów.
Zapytam wprost – nie będzie pani podawała trofinetide dzieciom z zespołem Retta?
M.Ch.K.: – Nie będę, dopóki nie będę miała wystarczających danych dotyczących tego leku. W przypadku terapii genowej w leczeniu SMA wiedziałam wszystko: jakich efektów możemy się spodziewać, jakie mogą wystąpić działania niepożądane, jaki jest dokładny mechanizm działania. W tym przypadku mam natomiast jakiś lek, którego mechanizmu działania do końca nie znam. Równie dobrze może być on taki sam jak zwykłego pirocetamu – neuroprotekcyjne działanie ochronne na ośrodkowy układ nerwowy. Pirocetam można kupić w każdej aptece za grosze, a nie za miliony. Co nie zmienia faktu, że wiem, że jeśli nie zrobimy tego w Polsce, to ci rodzice pojadą z dziećmi do Stanów Zjednoczonych, co oznacza, że poniosą dodatkowe koszty związane z lotem i zakwaterowaniem.
R.J.: – Rodzice pojadą do USA, ponieważ nie analizują tej sytuacji w taki sposób, jak my ją analizujemy.
A.F.: – Mają pieniądze na rok, dwa czy trzy lata terapii? Pewnie nie będzie ich stać na kilkadziesiąt podań. Pytanie, co potem?
R.J.: – Gdy rozmawiam z rodzicami, to mówią: „Na rok uzbieraliśmy i zobaczymy, czy będzie działać, bo jeśli nie, to przestaniemy podawać ten lek”. A ja pytam: A co wiemy na temat przerwania terapii? Otóż nic o tym nie wiemy.
M.Ch.K.: – A co wiemy na temat długoterminowego stosowania terapii? Również nic.
Pani nie rekomenduje rodzicom podawania tego leku. Co w tej sytuacji ma zrobić minister zdrowia?
A.F.: – Mamy całkiem niezłą procedurę podejmowania decyzji refundacyjnej. Minister nie ma wpływu na to, czy zostanie złożony wniosek refundacyjny, czy nie – chociaż uważam, że to nie jest do końca w porządku, bo jeżeli się pojawia nowa technologia, to złożenie wniosku powinno być obowiązkiem podmiotu odpowiedzialnego. Jeśli zostanie złożony, to rozpoczyna się procedura oceny. I wchodzi do gry Agencja Oceny Technologii Medycznych i Taryfikacji. Ona na te wszystkie wątpliwości, o których dziś mówiliśmy – czyli dotyczące jakości materiału dowodowego, jakości badań klinicznych wziętych pod uwagę przy rejestracji – popatrzy pod kątem refundacji.
Zawsze podkreślam, że procedury rejestracyjne różnią się od refundacyjnych, bo czym innym jest dopuszczenie do obrotu i stworzenie warunków do zbadania, jak lek działa, gdy się go używa zgodnie ze wskazaniami rejestracyjnymi, a czym innym jest decyzja o tym, żeby wydawać na coś pieniądze publiczne.
R.J.: – I to jest świetna konkluzja. Wniosek mój jest taki, że minister zdrowia powinien skierować tę technologię do oceny przez AOTMiT. A agencja oceniłaby jej wartość kliniczną i finansową, po czym wszem i wobec opublikowałaby swój raport. I to zarówno w języku dla terapeutów, jak i dla rodziców. Byłoby to wyrażeniem przez ministra troski o chore dzieci, których rodzicom dziś przychodzi do głowy, żeby pojechać od Stanów Zjednoczonych.
Szef resortu zdrowia jest przecież również od tego, by obywateli informować, budować świadomość, zapobiegać ryzykom i niebezpieczeństwom. Ma ku temu instrumenty.
M.Ch.K.: – W ten sposób minister otoczyłby opieką nie tylko rodziców, ale też lekarzy chcących tę technologię zastosować. Nie zostawiałby ich dłużej samych na zasadzie: „Róbcie sobie, co chcecie, a potem to wy bierzcie za to odpowiedzialność”.
A.F.: – Autorytet regulatora powinien być w tej sytuacji dobrze wykorzystany. Skierowanie do AOTMiT powinno się pojawić przy pierwszym wniosku o zrefundowanie leku w imporcie docelowym.
M.Ch.K.: – Powiem przewrotnie – jeśli to miałoby ministra do tego skłonić, mogę taki wniosek napisać.
A.F.: – Konkludując: rozmawialiśmy również o idei europejskiego zdrowia i warto zwrócić uwagę, że mamy przykłady udanej współpracy państw członkowskich…
Na poziomie unijnym negocjowano ceny szczepionek przeciwko COVID-19.
A.F.: – Otóż to. A zatem ewentualność prowadzenia negocjacji i ustalania cen na poziomie europejskim istnieje. I wydaje mi się, że powinna być wykorzystywana częściej.
R.J.: – Chodzi wszak o zapobieganie rozbójniczemu działaniu na rynku leków. A na już rekomendujemy – niech AOTMiT oceni trofinetide. Rodzice w całej Europie wypatrują, czy lek zostanie zarejestrowany również u nas. A kiedy to się stanie, to wydarzy się to samo, co w USA – pojawią się nagłówki: „Jest lek na zespół Retta”. Co jest nieprawdą.
M.Ch.K.: – Nieprawdą.
R.J.: – Tym bardziej minister zdrowia powinien działać teraz. Zanim lek zostanie zarejestrowany. Agencja powinna mieć już w ręku raport i ogłosić, jak ocenia ten lek. Ja go nie dyskryminuję. Może w jakiś sposób działa, jednak moim zdaniem nie jest wart miliona i informacja medialna, jaka się w związku z nim pojawiła, jest nieprawdziwa.
Dla rodziców chorych dzieci najistotniejsze jest poczucie, że robią dla nich wszystko, co najlepsze. Pani profesor, proszę – jako autorytet – powiedzieć, czy nie zbierając miliona złotych na nowy lek, mogą mieć takie poczucie?
M.Ch.K.: – Według mnie zdecydowanie tak. Z pełną odpowiedzialnością mogę powiedzieć, że nie znamy do końca mechanizmu działania tego leku, badania są zbyt mało precyzyjne i przeprowadzono je na zbyt małej grupie chorych. Dopóki nie będziemy mieli więcej danych, podchodziłabym do leczenia tym lekiem bardzo ostrożnie.